
QUIMICAGIMNASIANO TABLA CON NÚMEROS DE OXIDACIÓN GRADO OCTAVO (IMPRIMIR)
Nota. Las masas atómicas de isótopos son cercanas pero no iguales a sus números de masa. Por ejemplo, \(\ce{^35_17Cl}\) tiene número de masa masa = 35, pero la masa atómica de este isótopo es 34.969 amu como se muestra en el ejemplo anterior. La masa atómica promedio ponderada suele estar más cerca del número de masa del isótopo más abundante, por ejemplo, 35.45 amu en el ejemplo.
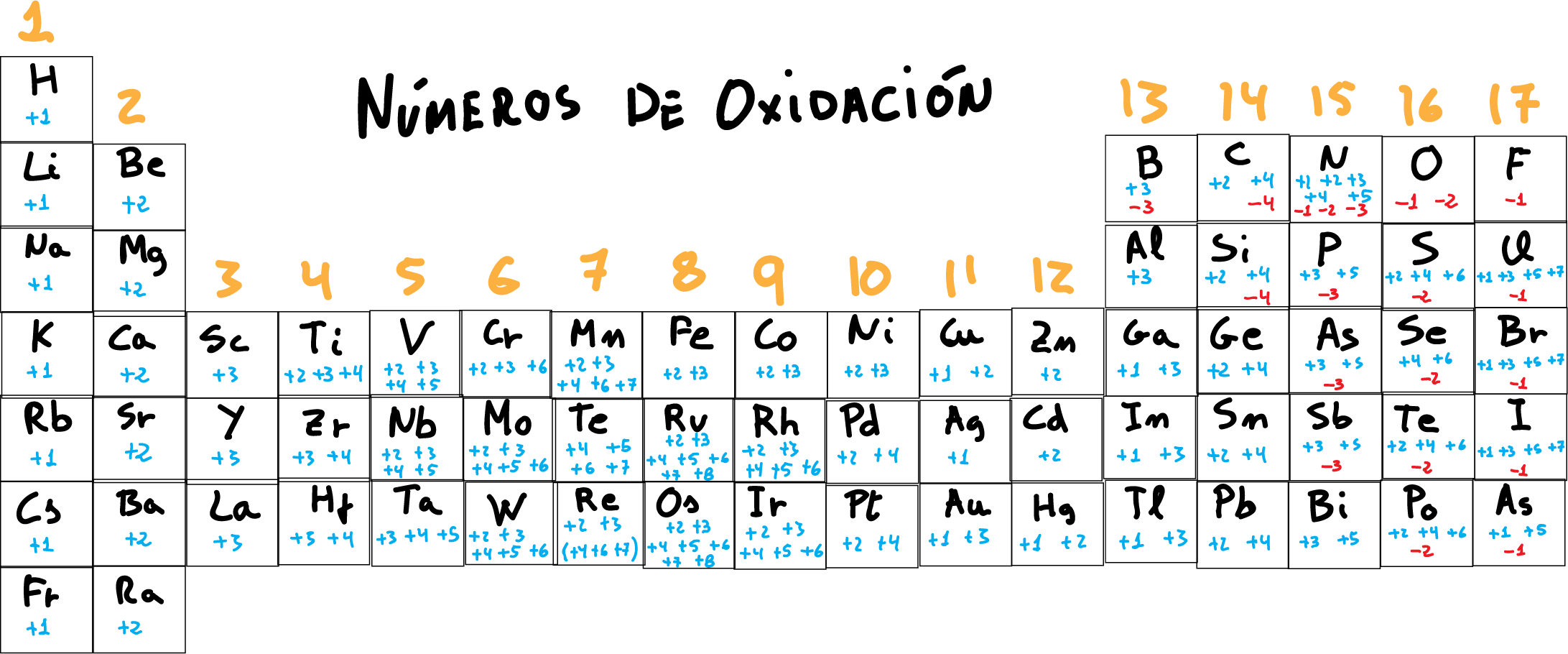
Número de Oxidación Definición, Cálculo De Química
1.El Número de Oxidación de todos los Elementos en Estado Libre, no combinados con otros, es cero (p. ej., Na, Cu, Mg, H2, O2, Cl2, N2). 2. El Número de Oxidación del Hidrógeno (H) es de +1, excepto en los hidruros metálicos (compuestos formados por H y algún metal), en los que es de -1 (p. ej., NaH, CaH2).

Tabla Numeros de Oxidacion PDF PDF
Los elementos del grupo 1 suelen tener un número de oxidación +1, mientras que los de la familia del calcio, zinc y aluminio presentan un número de oxidación de +2 y +3 respectivamente. Los elementos altamente electronegativos tienden a tener números de oxidación negativos, mientras que los menos electronegativos tienen números de.

Nomenclatura de los Compuestos Tabla números de oxidación
En la tabla tienes los números de oxidación más habituales de los elementos. Están relacionados con su situación en la tabla periódica y con las característias de los enlaces que forman, como ya viste en la unidades 1 y 2: por ejemplo, en los alcalinotérreos -grupo 2- es +2 porque como tienen dos electrones en la capa más externa tienen tendencia a perderlos para alcanzar la.

Números de Oxidación MÁS QUE APUNTES
Esta tabla nos permite entender mejor las interacciones entre los elementos y también nos proporciona información sobre la estructura y la naturaleza de los elementos. Para comprender mejor la tabla periódica, es importante conocer los diferentes tipos de elementos. Estos incluyen los metales, los no metales, los semimetales y los gases nobles.
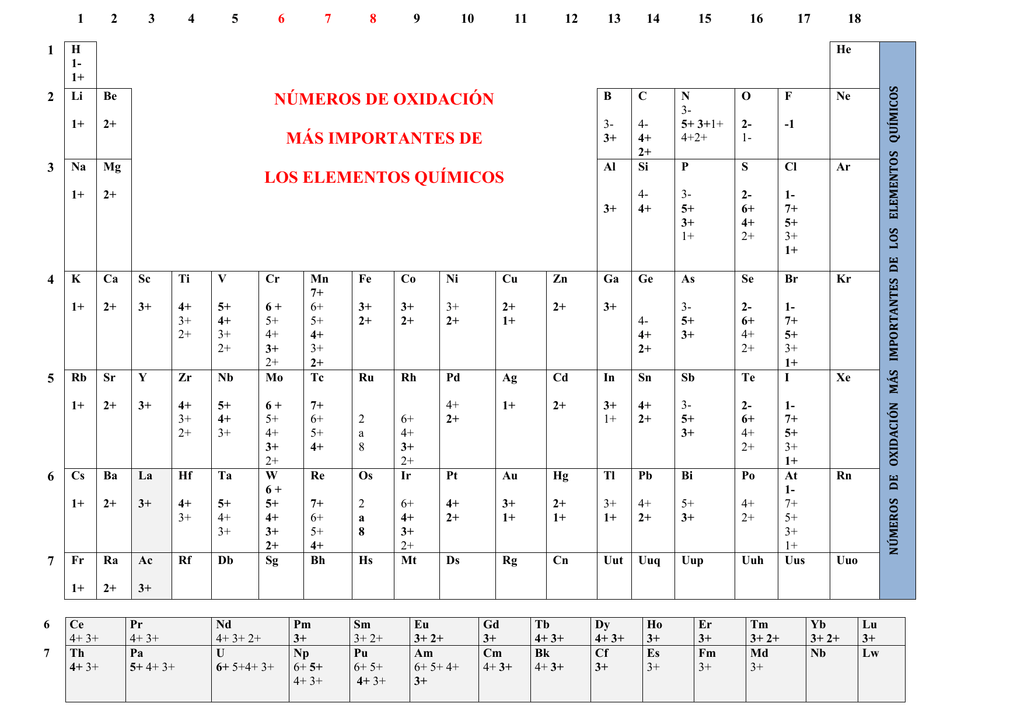
números de oxidación más importantes de los elementos químicos
Fr. +1. Ra. +2. * Los números de oxidación que aparecen entre paréntesis son con los que actúan cuando forman compuestos ternarios, actuando como no metales. ** El oxígeno solo funciona con el número de oxida. ción -1 en los peróxidos. *** Los no metales, cuando se combinan con el hidrógeno, actúan con el número de oxidación.
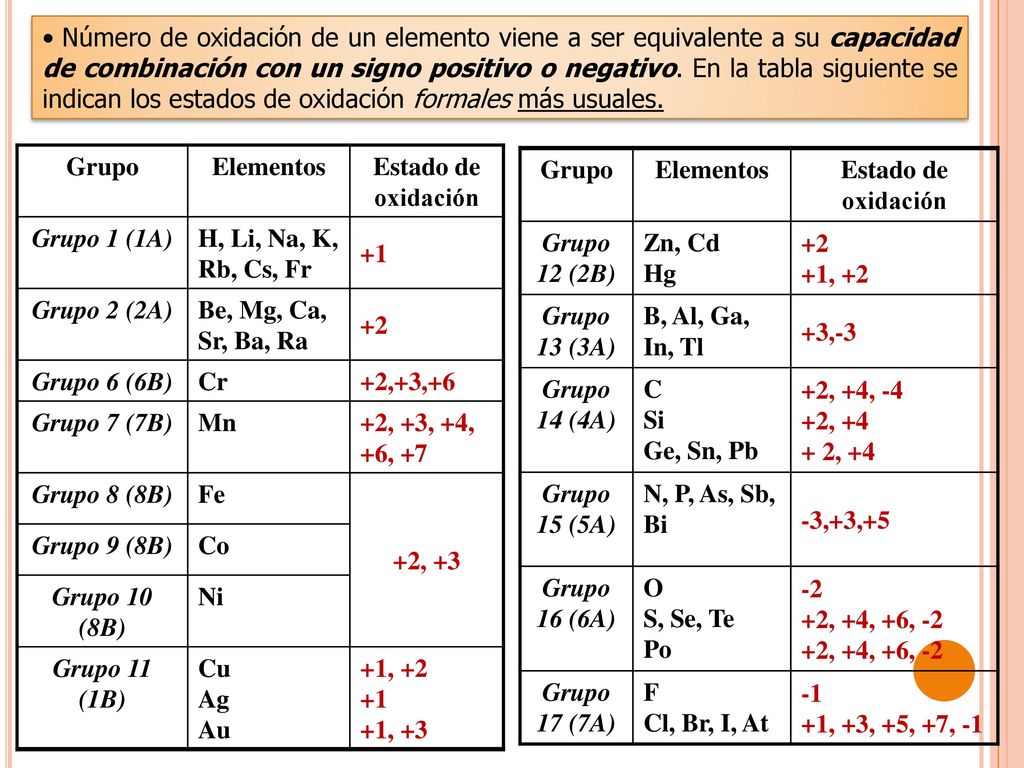
CIENCIA EN LA WEB Números de oxidación de los elementos químicos
Descubra los secretos de la tabla periódica con números de oxidación. La tabla periódica es una herramienta práctica para comprender la química. Está diseñada para mostrarnos la estructura de los elementos y cómo se relacionan entre sí. Los números de oxidación son una parte importante de la tabla periódica que nos ayuda a entender.

Quimica 2.2.5 Número de oxidación.
Los números de oxidación son una herramienta fundamental en la química que nos permite determinar el grado de carga de los átomos en un compuesto. Estos números representan la cantidad de electrones que un átomo ha ganado o perdido en una reacción química. Conocer los números de oxidación es esencial para comprender y predecir el.
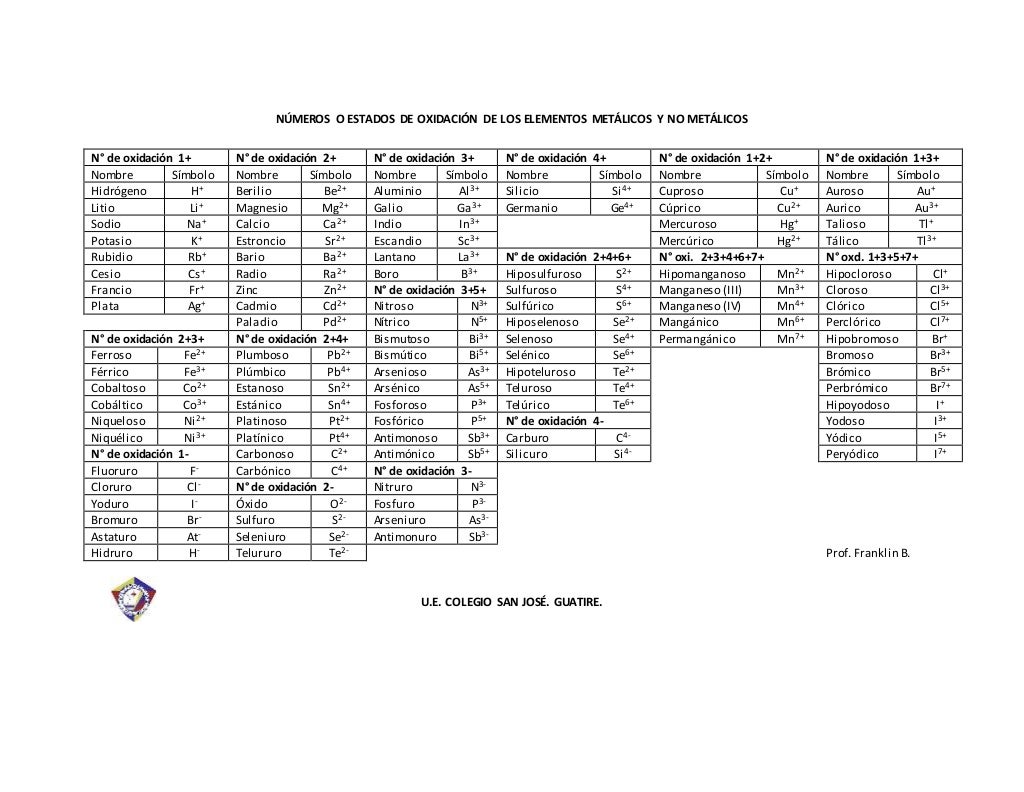
Números de oxidación y tabla de iones comunes el átomo
Aprende gratuitamente sobre matemáticas, arte, programación, economía, física, química, biología, medicina, finanzas, historia y más. Khan Academy es una organización sin fines de lucro, con la misión de proveer una educación gratuita de clase mundial, para cualquier persona en cualquier lugar.

numero de oxidacion de los elementos de la tabla periodica Brainly.lat
Tabla periódica con los números de oxidación En la siguiente figura se recopilan los números de oxidación del los elementos de la tabla periódica . Como característica general, los átomos alcalinos (grupo 1) presentan carga +1 , los alcalino-terreos (grupo 2), numero de oxidación +2 , y los halógenos cuando tienen número de oxidación negativo de -1 .

FÍSICA Y QUÍMICA "IES EUGENIO HERMOSO" Números de Oxidación
El hidrógeno (H) presenta número de oxidación +1 con los no metales y -1 con los metales. El flúor (F) sólo presenta el número de oxidación -1. El oxígeno (O) presenta el número de oxidación -2, excepto en los peróxidos donde es -1. Los metales alcalinos (grupo 1, o grupo del Li) tienen 1 electrón de valencia, tenderán a.

Resultado de imagen para tabla periodica completa con numeros de oxidacio… Tabla periodica de
Tabla periódica interactiva con páginas dinámicas que muestran nombres, electrones, estados de oxidación, tendencias, orbitales, isótopos y búsqueda. Descripciones completas.
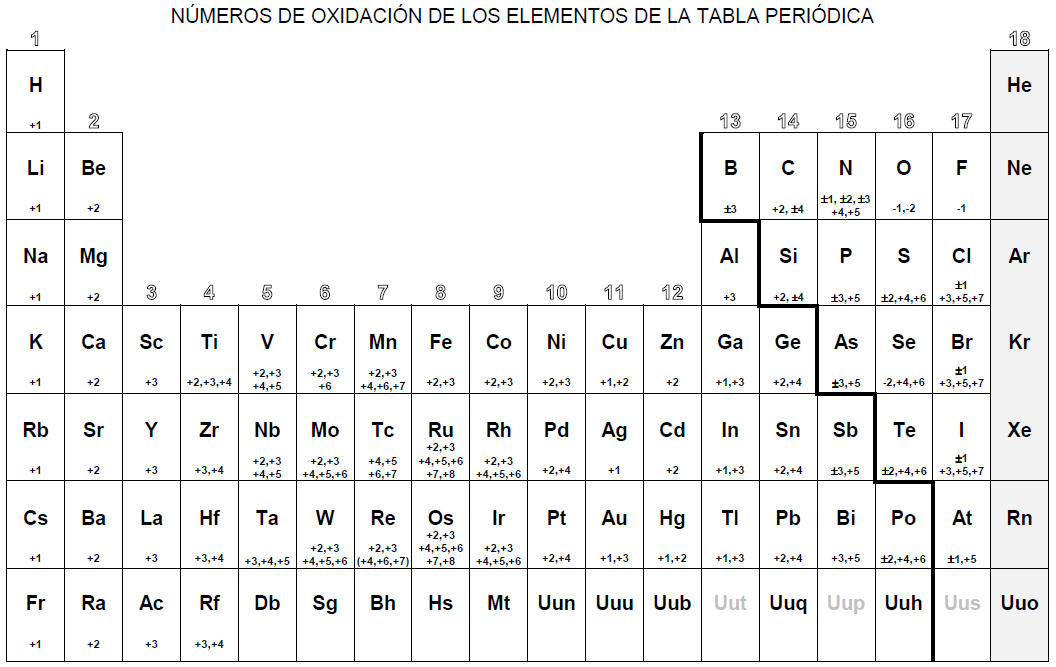
numero de oxidacion
La masa atómica se enumera en una tabla periódica como un número debajo del símbolo y nombre del elemento, como se ilustra en la Fig. 4.1.2. La masa atómica se enumera como un número sin unidad porque es la masa de un átomo en amu y también es la masa de un mol (masa molar) del átomo en gramos.
+18.32.30.png)
JANO SENSEI NÚMEROS DE OXIDACIÓN MÁS COMUNES DE LOS ELEMENTOS
Ejemplos de números de oxidación. Veamos ejemplos específicos de números de oxidación en diferentes compuestos. 1. Ácido clorhídrico (HCl): el número de oxidación del cloro es -1. 2. Sulfato de sodio (Na2SO4): el número de oxidación del azufre es +6. 3. Óxido de hierro (Fe2O3): el número de oxidación del hierro es +3.
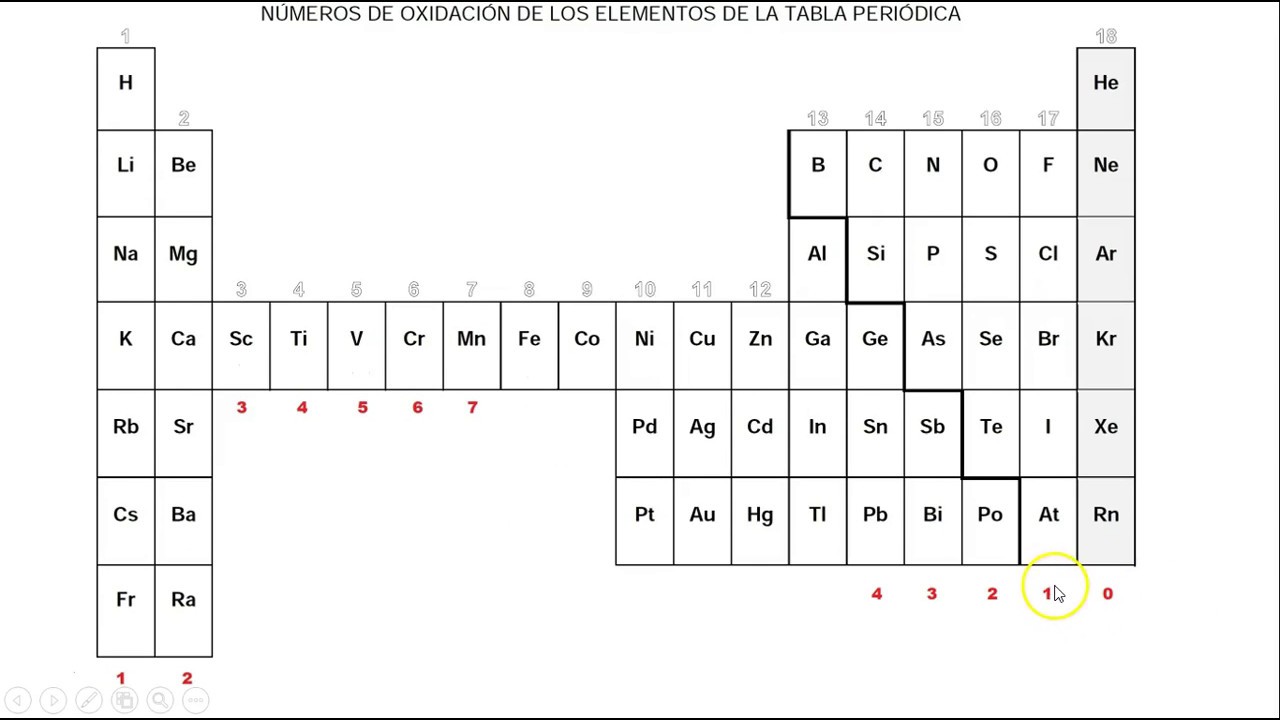
APRENDER LOS NÚMEROS DE OXIDACIÓN FÁCILMENTE YouTube
Cloro en compuestos con flúor u oxígeno: Debido a que el cloro adopta una variedad tan amplia de estados de oxidación en estos compuestos, es más seguro simplemente recordar que su estado de oxidación no es -1, y trabajar el estado correcto usando flúor u oxígeno como referencia. Ejemplo 11.16.1 11.16. 1 : Redox Reactions.
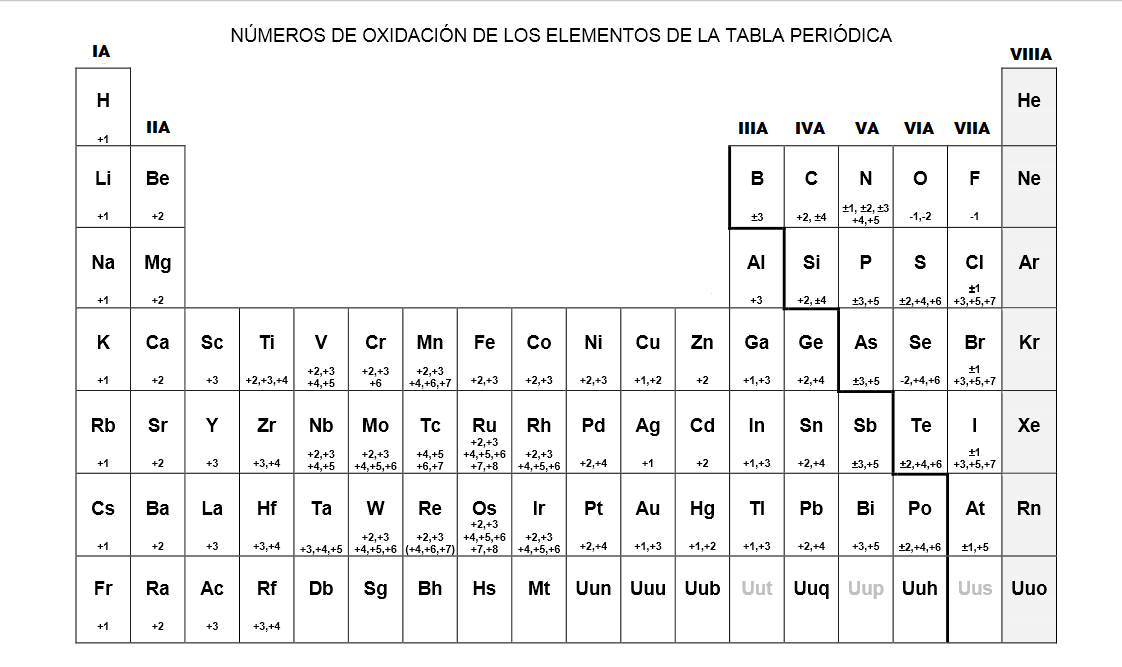
Nomenclatura de los Compuestos Tabla números de oxidación
Instrucciones. Enter the formula of a chemical compound to find the oxidation number of each element. A net ionic charge can be specified at the end of the compound between { and }. For example: ZnCl4 {2-} or NH2NH3 {+}. Enter just an element symbol to show the common and uncommon oxidation states of the element.